| �е������ਹ��������δ�͡��Ţͧ�������ԡ�����ǧ��ǹ�����ͫյ���������Ԥյ������ö������Ѻ���˹觡ѹ �·����㴵��˹���Ҩ���躹�ѹ�з�������˹���йҺ�����������йҺ����¢ͧǧ��ǹ���� ������ӵ�����е���ըӹǹ����������������ա�ͧ�ٻ��� ��ſ� ( α )- ����յ� ( ß )- ����դس���ѵԷҧ����Ҿᵡ��ҧ�ѹ�ҡ��� ������¡�ç�ٻ���ᵡ��ҧ�ѹẺ��ſ���кյҹ������� �������� (anomer) ��觡ѹ��Сѹ Show
มอนอแซ็กคาไรด์ (Monosaccharide) หรือน้ำตาลโมเลกุลเดี่ยว มีลักษณะเป็นโมเลกุลซึ่งประกอบด้วยธาตุคาร์บอน 3-8 อะตอม สามารถละลายน้ำได้ดีและมีรสหวาน เป็นน้ำตาลที่มีขนาดโมเลกุลเล็กที่สุดไม่สามารถถูกย่อยให้เล็กลงกว่านี้ได้ ร่างกายสามารถดูดซึมนำไปใช้ได้ทันที น้ำตาลโมเลกุลเดี่ยวสามารถแบ่งได้เป็นหลายชนิด ซึ่งแต่ละชนิดอาจมีสุตรโมเลกุลเหมือนกัน แต่มีสูตรโครงสร้างที่แตกต่างกันได้ เช่น ไรโบส ไลโซส ไซโลส และอะราบิโนส ซึ่งต่างก็มีสูตรโมเลกุลเป็น C5H10O5 เหมือนกัน แต่มีสูตรโครงสร้างที่แตกต่างกัน อัตราการเกิดปฏิกิริยาเคมี คือ ความเร็วที่ตัวทำปฏิกิริยาเปลี่ยนไปเป็นสารผลิตภัณฑ์ต่อหน่วยเวลา โดยที่หน่วยความเข้มข้นของสารเป็น mol/dm3 ดังนั้น อัตราการเกิดปฏิกิริยาเคมีจึงมีการเปลี่ยนแปลงความเข้มข้นของสารต่อวินาที ชั่วโมง หรือวัน ทั้งนี้ ขึ้นอยู่กับปฏิกิริยาเกิดเร็วหรือช้านั่นเอง
สรุปเนื้อหา อัตราการเกิดปฏิกิริยาเคมีอัตราการเกิดปฏิกิริยาเคมี สามารถจำแนกตามชนิดของปฏิกิริยา ได้ 2 ประเภท ได้แก่ 1. ปฏิกิริยาเนื้อเดียว (homogeneous reaction) ซึ่งจัดเป็นปฏิกิริยาที่สารตั้งต้นทั้งหมดอยู่ในสถานะเดียวกัน CH4(g)+ 2O2(g)—->CO2(g) + 2H2O(g) 2. ปฏิกิริยาเนื้อผสม (heterogeneous reaction) จัดเป็นปฏิกิริยาที่สารต่าง ๆ ไม่ได้อยู่ในสถานะเดียวกัน 3HCl(aq) + HNO3(aq)—>Cl2(g) + NOCl(g) + 2H2O(l) หมายเหตุ : การทราบชนิดของปฏิกิริยาจะทำให้ศึกษาปัจจัยที่มีผลต่ออัตราการเกิดปฏิกิริยานั้นได้ง่ายขึ้น
นอกจากนี้ ยังสมารถแบ่งประเภทอัตราการเกิดปฏิกิริยาเคมี ได้เป็น 3 แบบ ได้แก่ 1. อัตราการเกิดปฏิกิริยาเฉลี่ย (Average rate) คือ อัตราการเกิดปฏิกิริยาที่คิดจากการเปลี่ยนแปลงปริมาณสารตั้งต้นที่ลดลง หรือการเปลี่ยนแปลงปริมาณสารผลิตภัณฑ์ที่เพิ่มขึ้น ตั้งแต่เริ่มต้นปฏิกิริยาจนสิ้นสุดการเกิดปฏิกิริยา หรือสิ้นสุดการทดลองในหนึ่งหน่วยเวลา ซึ่งมีได้ค่าเดียว 2. อัตราการเกิดปฏิกิริยา ณ ขณะใดขณะหนึ่ง (Instantaneous rate) คือ อัตราการเกิดปฏิกิริยาที่คิดจากการเปลี่ยนแปลงปริมาณสารตั้งต้นที่ลดลง หรือการเปลี่ยนแปลงปริมาณสารผลิตภัณฑ์ที่เพิ่มขึ้น ณ ช่วงใดช่วงหนึ่ง ขณะที่ปฏิกิริยากำลังดำเนินอยู่ในหนึ่งหน่วยเวลาที่ช่วงนั้น ทั้งนี้ อัตราการเกิดปฏิกิริยานี้มีได้หลายค่า ที่เวลาต่างกันจะมีค่าไม่เท่ากัน นั่นคือ ตอนเริ่มต้นอัตราการเกิดปฏิกิริยาจะมีค่ามาก เมื่อปฏิกิริยาดำเนินต่อไป อัตราการเกิดปฏิกิริยาจะลดลงตามลำดับ เพราะความเข้มข้นของสารตั้งต้นลดลงนั่นเอง 3. อัตราการเกิดปฏิกิริยา ณ จุดใดจุดหนึ่งของเวลา คือ อัตราการเกิดปฏิกิริยาที่คิดจากการเปลี่ยนแปลงปริมาณสารตั้งต้นที่ลดลง หรือการเปลี่ยนแปลงปริมาณสารผลิตภัณฑ์ที่เพิ่มขึ้น ณ เวลาใดเวลาหนึ่งในช่วงสั้นๆ ขณะที่ปฏิกิริยากำลังดำเนินอยู่ในหนึ่งหน่วยเวลา อัตราการเกิดปฏิกิริยา ณ จุดใดจุดหนึ่งของเวลา หาได้โดยการนำข้อมูลที่ได้จากการทดลองไปเขียนกราฟ (ให้ปริมาณสารที่เปลี่ยนแปลงเป็นแกนตั้ง เวลาเป็นแกนนอน) เมื่อต้องการทราบอัตราการเกิดปฏิกิริยาที่เวลาใด ก็ให้ลากเส้นตั้งฉากตรงจุดเวลานั้นไปตัดเส้นกราฟลากเส้นสัมผัสให้ผ่านจุดตัด แล้วหาค่าความชัน (Slope) ของเส้นสัมผัส ซึ่งอัตราการเกิดปฏิกิริยา ณ ขณะนั้นก็ดูจากค่าความชันนั่นเอง
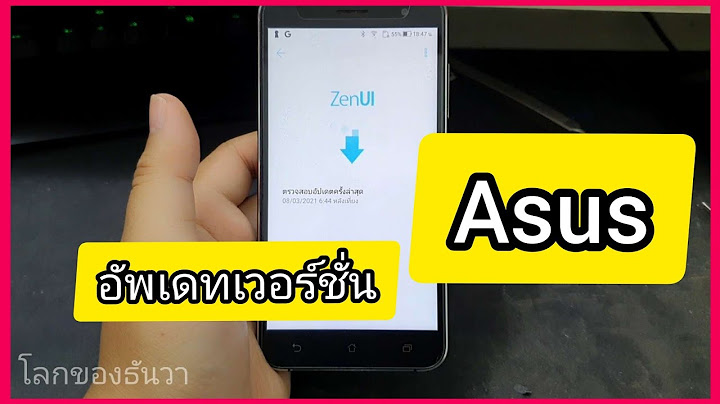
ปัจจัยทีมีผลต่ออัตราการเกิดปฏิกิริยาเคมี มีหลากหลาย ดังนี้1. ธรรมชาติของสารตั้งต้น เพราะ สารต่างชนิดกันจะสามารถเกิดปฏิกิริยาได้เร็วหรือช้านั้น ขึ้นอยู่กับสมบัติเฉพาะตัวของสารแต่ละชนิด เช่น โลหะโซเดียมทำปฏิกิริยากับน้ำเย็นได้เร็วมาก และเกิดปฏิกิริยารุนแรง ในขณะที่โลหะแมกนีเซียมทำปฏิกิริยากับน้ำเย็นได้ช้า แต่เกิดได้เร็วขึ้นเมื่อใช้น้ำร้อน ทั้งนี้ มีสาเหตเนื่องมาจาก โลหะโซเดียมมีความว่องไวในการเกิดปฏิกิริยาดีกว่าโลหะแมกนีเซียม สารบางชนิดจะทำปฏิกิริยาได้ยาก ยกตัวอย่างเช่น การสึกกร่อนของหิน การเกิดสนิมเหล็ก แต่ในทางกลับกันบางชนิดก็ทำปฏิกิริยาได้ง่าย เช่น การระเบิดของประทัด 2. ความเข้มข้นของสารตั้งต้น เพราะโดยปกติแล้วปฏิกิริยาเคมีโดยทั่ว ๆ ไป อัตราการเกิดปฏิกิริยาเคมี มักขึ้นอยู่กับความเข้มข้นของสารตั้งต้นที่เข้าทำปฏิกิริยา เช่น ปฏิกิริยาระหว่างโลหะกับกรด ถ้าเริ่มต้นใช้กรดที่มีความเข้มข้นสูงจะเกิดการกัดกร่อนโลหะได้เร็วกว่ากรดที่มีความเข้มข้นต่ำ เป็นต้น อัตราการเกิดปฏิกิริยานั้น อาจขึ้นอยู่กับความเข้มข้นของสารตั้งต้นเพียงสารใดสารหนึ่งหรือทุกสารก็ได้ แต่อย่างไรก็ตาม ห็ยังมีมีปฏิกิริยาเคมีบางชนิดที่อัตราการเกิดปฏิกิริยาไม่ขึ้นอยู่กับความเข้มข้นของสารตั้งต้น โดยไม่ว่าจะเปลี่ยนความเข้มข้นของสารตั้งต้นอย่างไร อัตราการเกิดปฏิกิริยาคงที่เสมอ เช่น ปฏิกิริยาการกำจัดแอลกอฮอล์ในเลือดของคน เป็นต้น 3.พื้นที่ผิวของสารตั้งต้น โดยปัจจัยนี้จะมีอิทธิพลต่ออัตราการเกิดปฏิกิริยาเคมีก็ต่อเมื่อปฏิกิริยาเคมีที่เกิดขึ้นนั้นเป็นปฏิกิริยาเคมีแบบเนื้อผสมที่มีสารตั้งต้นเป็นของแข็งร่วมอยู่ด้วย เช่น การเกิดปฏิกิริยาระหว่าง Mg และ HCl กล่าวคือ ปฏิกิริยาของโลหะแมกนีเซียมกับกรดไฮโดรคลอริกจะเกิดแก๊สไฮโดรเจน ซึ่งถ้าทำให้ลวดแมกนีเซียมเป็นชิ้นเล็ก ๆ จะพบว่าปฏิกิริยานั้นเกิดเร็วกว่าลวดแมกนีเซียมที่เป็นแผ่นหรือขดเป็นสปริง 4.อุณหภูมิ โดยเมื่ออุณหภูมิสูงขึ้น อัตราการเกิดปฏิกิริยาก็จะเพิ่มขึ้นด้วย เช่น การบ่มผลไม้ในภาชนะที่มีฝาปิด จะสุกเร็วกว่าการไว้ข้างนอก 5. ตัวเร่งปฏิกิริยา (Catalyst) คือ สารที่เติมลงไปในปฏิกิริยาแล้วทำให้ปฏิกิริยาเกิดได้เร็วขึ้น หรือทำให้อัตราการเกิดปฏิกิริยาเกิดได้เพิ่มขึ้น โดยที่ตัวเร่งปฏิกิริยาอาจจะมีส่วนร่วมในการเกิดปฏิกิริยาหรือไม่ก็ได้ แต่เมื่อสิ้นสุดปฏิกิริยา ตัวเร่งปฏิกิริยาเหล่านี้จะต้องมีปริมาณเท่าเดิมและมีสมบัติเหมือนเดิม 6. ตัวหน่วงปฏิกิริยา (Inhibiter) คือ สารที่เติมลงไปในปฏิกิริยาแล้วทำให้ปฏิกิริยาเกิดช้าลง หรือทำให้อัตราการเกิดปฏิกิริยาช้าลง และเมื่อสิ้นสุดปฏิกิริยา ตัวหน่วงปฏิกิริยาจะกลับคืนมาเหมือนเดิมและมีมวลคงที่ แต่สมบัติทางกายภาพเปลี่ยนแปลงไป เช่น ขนาด รูปร่าง โดยปกติแล้ว การเกิดปฏิกิริยาเคมีจะต้องมีพลังงานเข้ามาเกี่ยวข้องด้วย ซึ่งการดำเนินไปของปฏิกิริยาในแง่ของพลังงานของโมเลกุลเมื่อโมเลกุลของก๊าซมาชนกันจนกระทั่งกลายเป็นผลิตภัณฑ์สามารถจะแสดงให้เห็นได้โดยอาศัยกราฟซึ่งจะแสดงความสัมพันธ์ระหว่างพลังงานของสารตั้งต้นพลังงานก่อกัมมันต์ของปฏิกิริยา และพลังงานของผลิตภัณฑ์ดังนี้ ก. ปฏิกิริยาระหว่าง NO2 กับ CO ซึ่งเป็นประเภทคายความร้อน 
จากรูปนี้ การเปลี่ยนแปลงพลังงานของปฏิกิริยา NO2 + CO → NO + CO2
ข . ปฏิกิริยา 2HI(g) → H2 ( g) + I2 (g) ซึ่งเป็นปฏิกิริยาประเภทดูดความร้อน 
กฎอัตรา คืออะไรกฎอัตรา (Rate law) คือ สมการที่แสดงความสัมพันธ์ระหว่างอัตราการเกิดปฏิกิริยากับค่าคงที่อัตราและความเข้มข้นของสารตั้งต้น ซึ่งกฎอัตราจะมีประโยชน์มาก ถ้าเรารู้ค่าคงที่อัตราและความเข้มข้นของสารตั้งต้นแล้ว เราก็สามารถคำนวณอัตราการเกิดปฏิกิริยาจากกฎอัตราได้ ในทางกลับกัน เราสามารถที่จะใช้สมการนี้ในการหาความเข้มข้นของสารตั้งต้น ณ เวลาใดๆ ในขณะที่เกิดปฏิกิริยาได้ด้วย
กลไกของปฏิกิริยาเคมีElememtary reaction คือ ปฏิกิริยาที่เกิดขึ้นในขั้นตอนเดียว และอันดับของปฏิกิริยาจะเท่ากับจำนวนโมเลกุลอะตอมของสารตั้งต้นที่เข้าทำปฏิกิริยา ดังนั้น อันดับปฏิกิริยาของ Elememtary reaction จึงเรียกว่า “molecularity” โดย Elementary reaction ที่มี molecularity เป็น 1 เรียกว่า umimolecular reaction, 2 เรียกว่า bimolecular reaction และ 3 เรียกว่า termolecular reaction หมายเหตุ : Elementary reaction ที่มี molecularity มากกว่า 2 เกิดขึ้นได้ยากมาก ดังนั้น ปฏิกิริยาใดที่มี molecularity ตั้งแต่ 2 ขึ้นไป น่าจะไม่ใช่ elementary reaction
ตัวอย่างข้อสอบ เรื่อง อัตราการเกิดปฏิกิริยาเคมี1. CH3OH ทำปฏิกิริยากับ HCl เกิดเป็น CH3Cl และ H2O เมื่อวัดความเข้มข้นของ HCl ในขณะเกิดปฏิกิริยาได้ผลดังแสดงในตารางต่อไปนี้ เวลา ( s)ความเข้มข้นของ HCl ( mol/l)080 159 314 628 1.851.66 1.53 1.31 1.02 อัตราการเกิดปฏิกิริยาในช่วงเวลา 159 – 314 เป็นเท่าใด ก. 0.0014 mol/l/s
2. จากโจทย์ข้อ 1 อัตราการเกิดปฏิกิริยา เฉลี่ยเป็นเท่าใด ก. 0.0014 mol/l/s
3. ข้อความต่อไปนี้ข้อใดไม่ถูกต้อง ก. คะตะไลต์เมื่อใส่ลงไปในปฏิกิริยาทำให้อัตราการเกิดปฏิกิริยาเคมีเร็วขึ้น
4. ข้อใดมีผลทำให้อัตราการเกิดปฏิกิริยาเคมีเปลี่ยนแปลงไปในทิศทางเดียวกัน ก. เพิ่มอุณหภูมิ ลดความดัน
5. ปฏิกิริยา A(s) + B(aq) ———–> C(aq) + D(aq) เป็นปฏิกิริยาคายความร้อน การกระทำทั้งหมดในข้อใดทำให้อัตราการเกิดปฏิกิริยาเพิ่มขึ้น ก. ลดขนาดของ A เติมตัวเร่งปฏิกิริยา เพิ่มอุณหภูมิ
เคมี ม. ปลาย ต้องเรียนเรื่องอะไรบ้างการเรียน เคมี ม.ปลาย ตั้งแต่เคมี ม.4 เคมี ม.5 หรือ เคมี ม.6 นอกจากเรื่องอัตราการเกิดปฏิกิริยาเคมีที่จะต้องเจอแล้ว การเรียนวิชานี้ยังครอบคลุมไปถึงเรื่องอื่น ๆ ด้วย ไม่ว่าจะเป็นเรื่องโครงสร้างอะตอมและตารางธาตุ, พันธะเคมี, สมบัติของธาตุและสารประกอบ, โมลและสูตรเคมี, สารละลาย, ปริมาณสารสัมพันธ์, ของแข็ง ของเหลว ก๊าซ, แก๊สและสมบัติของแก๊ส, สมดุลเคมี, กรด-เบส, ไฟฟ้าเคมี, เคมีอินทรีย์, พอลิเมอร์, เชื้อเพลิงและซากดึกดำบรรพ์, เคมีกับการแก้ปัญหา, สารชีวโมเลกุล และอื่น ๆ ดังนั้น ใครที่กำลังเตรียมตัวจะเลือกเรียนสายวิทย์ หรือกำลังเรียนสายวิทย์อยู่ ก็จะต้องเจอกับการเรียนเรื่องต่าง ๆ เหล่านี้อย่างแน่นอน
 คอร์สเรียน เคมี อัตราการเกิดปฏิกิริยาเคมี ตัวต่อตัวเป็นคอร์สเรียนที่ผู้เรียนสามารถออกแบบการเรียนให้เหมาะกับตัวเองได้เป็นอย่างดี ไม่ว่าจะเรียนเพื่อติวสอบปลายภาค, ติวเพิ่มเกรด, กวดวิชาเข้ามหาวิทยาลัย ก็สามารถเลือกได้ตามแบบที่เราต้องการได้ด้วยหลักสูตรจำนวน 10 ชม. แต่หากใครที่พื้นฐานอ่อนหรืออยากมาเรียนเนื้อหาล่วงหน้าก็สามารถเพิ่มชั่วโมงเรียนให้เหมาะสมกับเราได้ น้ำตาลโมเลกุลเดี่ยว มีอะไรบ้างโมเลกุลเดี่ยว ได้แก่ กลูโคส (glucose) ฟรักโทส (fructose) และ กาแลคโทส (galactose) น้ำตาลโมเลกุลเดี่ยว 2 โมเลกุล สามารถเชื่อมเข้าด้วยกันเป็นไดแซคคาไรด์ (disaccharide)
น้ำตาลอะไรไม่ใช่น้ำตาลโมเลกุลเดี่ยวน้ำตาลโมเลกุลคู่ที่พบในอาหาร ได้แก่ น้ำตาลซูโครส (sucrose)
สารในข้อใดใช้ทดสอบน้ำตาลโมเลกุลเดี่ยว*การทดสอบน้ำตาลโมเลกุลเดี่ยว ใช้สารละลายเบเนดิกต์ จะได้ตะกอน สีแดงอิฐของCu2O ซึ่งใช้ตรวจน้ำตาลในปัสสาวะสำหรับคนเป็นโรคเบาหวาน *การทดสอบแป้งใช้สารละลายไอโอดีนให้สารละลายสีน้ำเงิน *น้ำตาลโมเลกุลคู่และพอลิแซ็กคาไรด์ไม่ให้ผลกับสารละลายเบเนดิกต์
น้ำตาลเฮกโซส มีอะไรบ้างแอลโดเฮกโซส (aldohexose) เป็นน้ำตาลที่มีจำนวนคาร์บอน 6 อะตอม และมีหมู่แอลดีไฮด์อยู่ในโมเลกุล เช่น น้ำตาลกลูโคสและกาแล็กโทส
|

กระทู้ที่เกี่ยวข้อง
การโฆษณา
ข่าวล่าสุด
การโฆษณา
ผู้มีอำนาจ
การโฆษณา
ถูกกฎหมาย
ช่วย

ลิขสิทธิ์ © 2024 th.ketiadaan Inc.