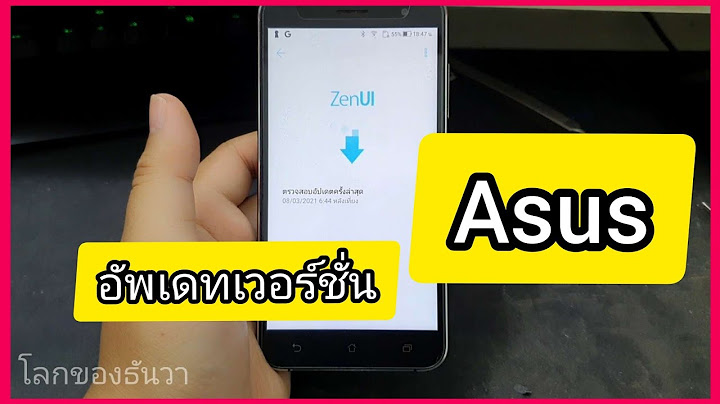
1. ของแข็ง (solid) คือ สารที่มีรูปร่างและปริมาตรที่แน่นอน ไม่เปลี่ยนแปลงตามภาชนะ อนุภาคชิดกันเป็นระเบียบ มีความหนาแน่นและแรงยึดเหนี่ยวระหว่างโมเลกุลสูงกว่าของเหลวและก๊าซ 2. ของเหลว (liquid) คือ สารที่มีปริมาตรแน่นอน แต่มีรูปร่างไม่แน่นอนเปลี่ยนแปลงตามภาชนะที่บรรจุ อนุภาคอยู่ใกล้เคียงกันแต่ไม่เป็นระเบียบ มีการชนกันตลอดเวลา จึงมีความหนาแน่นสูงกว่าก๊าซ 3. ก๊าซ (gas) คือ สารที่มีรูปร่างและปริมาตรไม่แน่นอน เปลี่ยนแปลงตามภาชนะที่บรรจุเพราะมีแรงยึดเหนี่ยวระหว่างโมเลกุลน้อยมาก จึงฟุ้งกระจายได้เต็มภาชนะและมีความหนาแน่นต่ำ ภาพแสดงการจัดเรียงอนุภาคของก๊าซ ระบบและการเปลี่ยนแปลงของสาร ระบบ (system) หมายถึง สิ่งที่อยู่ภายในขอบเขตที่ต้องการศึกษา การกำหนดองค์ประกอบของระบบ ขึ้นอยู่กับจุดมุ่งหมายของการศึกษา ซึ่งต้องกำหนดหรือระบุให้ชัดเจน สิ่งแวดล้อม (environment) หมายถึง สิ่งต่างๆ ที่อยู่นอกขอบเขตที่ต้องการศึกษา ตัวอย่างการกำหนดองค์ประกอบของระบบ เช่น การศึกษาการละลายของน้ำตาลทรายในน้ำ โดยสารละลายน้ำตาลทรายจะเป็นระบบ ส่วนบีกเกอร์ ภาชนะ และแท่งแก้วจัดเป็นสิ่งแวดล้อม ภาวะของระบบหมายถึง สมบัติต่าง ๆ ของสาร และปัจจัยที่มีผลต่อสมบัติของระบบ เช่น ความดันบรรยากาศ อุณหภูมิ ปริมาณของสาร เมื่อระบบเกิดการเปลี่ยนแปลงแล้วจะมีการถ่ายเทพลังงานระหว่างระบบกับสิ่งแวดล้อม ดังนี้ ประเภทของระบบ การเปลี่ยนแปลงพลังงานระหว่างระบบและสิ่งแวดล้อม จะใช้การถ่ายเทมวลของสารเป็นเกณฑ์ในการแบ่งประเภทของระบบ ดังนี้
การเปลี่ยนแปลงพลังงานของระบบ การเปลี่ยนแปลงพลังงานของระบบมี 2 ประเภท คือ 1. การเปลี่ยนแปลงประเภทคายความร้อนหรือประเภทคายพลังงาน คือ การเปลี่ยนแปลงที่ระบบคายพลังงานให้แก่สิ่งแวดล้อม เนื่องจากระบบมีอุณหภูมิสูงกว่าสิ่งแวดล้อม จึงถ่ายเทพลังงานจากระบบไปสู่สิ่งแวดล้อม เช่น การละลายของโซดาไฟในน้ำ อุณหภูมิของสารละลายสูงขึ้น จึงถ่ายเทพลังงานให้กับสิ่งแวดล้อม เพื่อทำให้อุณหภูมิของระบบลดลงจนอุณหภูมิของระบบเท่ากับอุณหภูมิของสิ่งแวดล้อม ดังภาพ 2. การเปลี่ยนแปลงประเภทดูดความร้อนหรือประเภทดูดพลังงาน คือ การเปลี่ยนแปลงที่ระบบดูดพลังงานจากสิ่งแวดล้อม เนื่องจากระบบมีอุณหภูมิต่ำกว่าสิ่งแวดล้อม ระบบจะปรับตัวโดยดูดพลังงานความร้อนจากสิ่งแวดล้อมเข้าสู่ระบบ เพื่อทำให้อุณหภูมิของระบบเท่ากับอุณหภูมิของสิ่งแวดล้อม เช่น การละลายของเกลือแกงในน้ำ อุณหภูมิของสารละลายต่ำลง จึงดูดพลังงานเข้าสู่ระบบ เพื่อทำให้อุณหภูมิของระบบสูงขึ้นจนอุณหภูมิของระบบเท่ากับอุณหภูมิของสิ่งแวดล้อม ภาพแสดงการ เปลี่ยนแปลงพลังงานของระบบ การเปลี่ยนสถานะของสาร สารต่างๆ อาจอยู่ในสถานะก๊าซ ของเหลว หรือของแข็งก็ได้ ขึ้นอยู่กับชนิดของสาร สารแต่ละชนิดจะมีจุดเดือดและจุดหลอมเหลวต่างกัน ซึ่งเป็นคุณสมบัติเฉพาะตัวของสาร การเปลี่ยนแปลงอุณหภูมิจะมีผลต่อการเปลี่ยนแปลงสถานะของสาร โดยที่พิจารณาตามหลักการ ดังภาพ  - การเปลี่ยนแปลงของสารจากสถานะของแข็งเป็นของเหลว เรียกว่า การหลอมเหลว อุณหภูมิขณะนั้นจะคงที่เรียนกว่า จุดหลอมเหลว พลังงานกับการเปลี่ยนแปลงของระบบ 1. พลังงานกับการเปลี่ยนสถานะ สารมี 3 ลักษณะ คือ ของแข็ง , ของเหลว และก๊าซ 2. พลังงานกับการละลายในการละลายเกิดจากสารตั้งแต่ 2 ชนิดขึ้นไปมาผสมเป็นเนื้อเดียวกันโดยไม่เกิดปฏิกิริยา ก.
อนุภาคของแข็งแยกตัวออกเป็นอนุภาคเล็ก ๆ ของแข็งมีจำนวนมากมายอยู่รวมกันโดยมีแรงยึดเหนี่ยวระหว่างกัน การแยกอนุภาคของแข็งออกจากเป็นอนุภาคเล็ก ๆ ต้องใช้พลังงาน (ดูดพลังงานจากสิ่งแวดล้อม) พลังงานนี้เรียกว่า " พลังงานแลตทิซ " (Lattice Energy) ผลการละลายน้ำของสารมีการเปลี่ยนแปลงพลังงานแบบใดจะต้องพิจารณาจากพลังงานแลตทิซ และพลังงานไฮเดรชัน ดังนี้
1. การเปลี่ยนแปลงแบบดูดความร้อน เมื่อพลังงานแลตทิซมากกว่าพลังงานไฮเดรชัน เช่น การละลายน้ำของโพแทสเซียมไนเตรต พลังงานกับการเปลี่ยนแปลงสถานะ การเปลี่ยนสถานะของสารเป็นการเปลี่ยนแปลงทางกายภาพ การเปลี่ยนสถานะของสารอาจเป็นการเปลี่ยนแปลงประเภทดูดพลังงานหรือคายพลังงาน ดังภาพ เมื่อสารได้รับความร้อนขณะที่มีการเปลี่ยนสถานะ อุณหภูมิของสารจะไม่มีการเปลี่ยนแปลง โดยจะนำ ความร้อนที่ได้รับไปใช้เปลี่ยนสถานะ ซึ่งเรียกค่าพลังงานที่นำไปใช้ในการเปลี่ยนแปลงของสารว่า ความร้อนแฝงจำเพาะของสาร สารแต่ละชนิดจะมีค่าความร้อนแฝงจำเพาะ 2 ค่าด้วยกัน คือ 1. ค่าความร้อนแฝงจำเพาะของการหลอมเหลว เป็นค่าพลังงานความร้อนที่นำมาใช้เปลี่ยนสถานะจากของแข็งเป็นของเหลว 2. ค่าความร้อนแฝงจำเพาะของการกลายเป็นไอ เป็นค่าพลังงานความร้อนที่นำไปใช้ในการเปลี่ยนสถานะจากของเหลวเป็นไอ - น้ำมีค่าความร้อนแฝงจำเพาะของการหลอมเหลว 80 แคลอรีต่อกรัม หมายความว่าในการทำน้ำแข็ง 1 กรัม ให้หลอมเหลวเป็นน้ำ ต้องใช้พลังงานความร้อน 80 แคลอรี พลังงานกับการเกิดปฏิกิริยาเคมี เมื่อสารเกิดปฏิกิริยาเคมีจะต้องมีสารใหม่เกิดขึ้นทุกครั้ง วิธีพิจารณาสารใหม่ให้สังเกตการเปลี่ยนสี กลิ่น และสิ่งใหม่ที่เกิดขึ้น เช่น ฟองก๊าซ , ตะกอน หรือควัน เป็นต้น การเกิดปฏิกิริยาเคมีจะต้องเกิด 2 ขั้นตอนเหมือนกับการละลายคือ ขั้นที่
1 ต้องสลายแรงยึดเหนี่ยวของสารตั้งต้น ( สารเดิม ) ซึ่งจะต้องใช้พลังงาน ( ดูดพลังงาน ) แยกอนุภาคของสารออกจากกัน การวัดความร้อน (Calorimetry) : การวัดความร้อนที่เปลี่ยนแปลงของปฏิกิริยาเคมี โดยใช้ “ Calorimeter ” q = ms  |

กระทู้ที่เกี่ยวข้อง
การโฆษณา
ข่าวล่าสุด
การโฆษณา
ผู้มีอำนาจ
การโฆษณา
ถูกกฎหมาย
ช่วย

ลิขสิทธิ์ © 2024 th.ketiadaan Inc.